在去年年底取消了对一致性评价设置的时限要求后,涉及4185个品种的仿制药一致性评价工作仍在加速推进。随着各地招采政策不断落地,多省市落实3家过评则不再采购未过评产品的政策,未过评产品面临被踢出全国市场的局面,仿制药大战一触即发。
丁香园Insight数据库数据显示,截至7月30日,目前共有300个品种、1334个仿制药一致性评价申请获受理,仅464个品种已处于BE实验以上进度,启动率仅11.18%。这其中,有230个受理号获通过,涉及87个品种、106家药企。其中,齐鲁制药已经超过华海药业成为目前一致性评价的最大赢家,共有14个品种获得通过,其次是复星医药(13个)、华海药业(11个)和中国生物制药(11个)。
一致性评价整体启动率仅11.18%
根据此前的政策规定,“289目录”中的仿制药,必须在2018年12月31日前完成一致性评价,否则将失去被医疗机构采购的机会。但是,在2018年12月28日,国家药品监督管理局发布《关于仿制药质量和疗效一致性评价有关事项的公告》(以下简称《公告》),对已经纳入国家基本药物目录的仿制药品种,不再统一设置一致性评价时限要求。化学仿制药应在首家品种通过一致性评价后3年内完成一致性评价。逾期未完成的,经申请认定后,可予以适当延期(原则上不超过5年)。逾期再未完成的,则不予再注册。
一致性评价进程包括参比制剂备案、药学研究、BE备案、开展BE试验和提供补充申请五个步骤。而开展BE试验是企业准备申报一致性评价的重要节点信号。据丁香园Insight数据库数据显示,截至7月30日,全部待评价的4185个品种中,有3473个品种暂无任何进度。以启动BE试验作为启动点计算,目前仅464个品种已处于BE实验以上进度,启动率只有11.18%,BE试验用时平均需要237天。“目前能做BE试验的机构太少,很多企业都在排队,应该增加这类机构的准入,有助于加速推进一致性评价工作。”北京鼎臣医药咨询管理中心负责人史立臣说。
从启动BE试验品种数量上来看,上药集团的品种最多,共有38个品种,其次为扬子江药业(25个)、复星医药(24个)、石药集团(19个)、白云山医药(18个)。
完成审核的受理号过评率68.05%
截至7月30日,一致性评价受理号共1334个,审核完毕的有338个,其中,有230个获批准,7个不批准通过,32个获批临床,69个未出结论,一致性评价通过率为68.05%。从国家药监局药品审评中心承办到通过,平均需要224天时间。
未通过的7个受理号中,有三个为白云山药业的产品,分别是白云山头孢氨苄、头孢拉定和羧甲司坦片;其余三个分别是英联生物的洛索洛芬钠、海正药业的他克莫司和国药的对乙氨基酚片。
在已通过品种所涉及的企业来看,排名靠前的均是我国医药研发实力较强的医药企业,其中,齐鲁制药成为了目前最大赢家,共有14个品种获通过,包括阿德福韦酯片、奥氮平片、富马酸替诺福韦二吡夫酯片等;复星医药紧跟其后,共有13个品种过评。去年一致性评价过评品种最多的华海药业排到了第三,有11个品种过评。
另外,根据上市药品目录集统计,有82个批准文号以新注册分类申报为由被纳入,视同通过一致性评价。
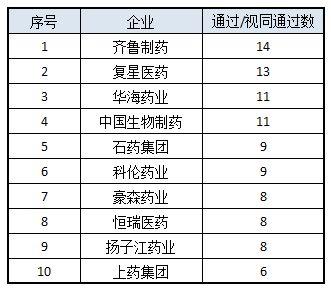
注:以上数据来自丁香园Insight数据库
25个品种已有三家及以上企业过评
按照国办2016年8号文要求,同一品种通过一致性评价企业数超过3家,则不再采购未通过一致评价公司的产品。目前,各省正在陆续落实上述政策,据不完全统计,已经有至少15个省份最新出台的集采政策中给出了上述规定。尤其是江西、江苏、黑龙江等多省市已经公示了部分因同品种药品过一致性评价生产企业达到3家以上,而暂停了未过评品种的挂网资格。
据丁香园Insight数据库数据显示,目前已有三家及三家以上企业通过的品种共有25个,已有两家企业通过的品种23个、仅一家企业通过的品种有91个(以上数据均包括视同通过一致性评价)。过评企业最多的品种是富马酸替诺福韦二吡夫酯片,包括中标企业成都倍特在内共有9家企业的该品种过评,其次为苯磺酸氨氯地平片(8个)、蒙脱石散(6个)等。而苯磺酸氨氯地平片和蒙脱石散分别还有28家和13家企业递交了一致性评价补充申请,通过在即。随着第二批“4+7”集采的酝酿,一场全国市场抢夺战即将拉开。(新京报)




请输入验证码